4.5. Теоретические расчеты адсорбции водорода углеродными наноматериалами
Механизм уникально высокой сорбции водорода углеродными наноматериалами пока неясен и рассматриваются разные модели сорбции: физическая адсорбция и хемосорбция молекул H2 на поверхности графенового листа, возникновение более чем одного слоя молекул Н2 между графеновыми слоями, капиллярная конденсация водорода внутри нанотрубок и в пространстве между графеновыми листами при аномально высоких температурах, электрически заряженное состояние водорода в углеродных наноматериалах. Соответственно, сильно различаются и результаты расчета максимальной водородной емкости наноматериалов.
В [107] с использованием метода Монте-Карло для углеродных материалов с щелевидными и цилиндрическими порами была рассчитана адсорбционная способность газообразного Н2 при различных температурах и давлениях водорода. Рассчитанные значения сорбции Н2 сопоставлены с экспериментальными данными, полученными для специально приготовленного микропористого активированного угля (АУ). Показано, что наблюдается линейная зависимость адсорбционной способности водорода от удельной поверхности АУ. Лучшие исследованные образцы АУ имели поверхность S=2290 м2/г, чему соответствовало максимальное значение адсорбции Н2, равное 0.6 % (мас.), которое хорошо согласуется с рассчитанным значением 0.7 % (мас.) Н2 для идеальных щелевидных пор с S = 2600 м2/г при 300 К и р=6 МПа [107]. Согласно [107], для адсорбции Н2 углеродным материалом при комнатной температуре и р=10 МПа оптимальными являются щелевидные поры с расстоянием
d = 0.7 нм. При этом наибольшее полученное значение объемной емкости Н2 равно 14 кг Н2/м3 (емкость по массе 1.3 %). По данным [107], практически во всем исследованном диапазоне температур и давлений сорбционная способность углеродного материала с щелевидными порами выше, чем с цилиндрическими. Отмечено, что при 77 К в порах с d = 1.0 нм может наблюдаться полимолекулярная (двухслойная) сорбция водорода даже при низких давлениях Н2, что соответствует гравиметрической емкости, равной ~ 2.0 и 5.5 % (мас.) Н2 для цилиндрических и щелевидных пор соответственно. Поэтому высокие значения поглощения Н2 однослойными НТ (5-10 % (мас.) Н2 при комнатной температуре), наблюдаемые в [71], не могут быть объяснены только физической адсорбцией, протекающей в НТ под действием капиллярных сил.
Расчеты [107] адсорбции Н2 при комнатной температуре и
= 11 МПа для щелевидных пор с d = 0.34 нм, соответствующим межплоскостному расстоянию для графеновых слоев в ГНВ [81], показывают, что водород не может адсорбироваться в таком материале. Поскольку при этих условиях гравиметрическая емкость по Н2 для углеродного материала с d = 0.7 нм составляет только 1.3 %, увеличение d в ходе поглощения водорода не может привести к значениям адсорбции Н2, сообщенным в [81] (11-67 %). Авторы в [108] также показали, что расстояния между графеновыми слоями d = 0.34 нм недостаточно для внедрения молекул водорода, а графитовым нановолокном с d = 0.9 нм при 298 К и 5-11.2 МПа может быть адсорбировано только 0.46-1.6 % (мас.) Н2.
Анализ адсорбции Н2 на поверхности графита с учетом условий сорбции, а также геометрических параметров молекулы водорода и слоя графита дает значение ~2.8 % (мас.) для одного слоя Н2, адсорбированного на единичном графеновом листе. В реальных системах межмолекулярные силы, взаимодействие молекул Н2 с поверхностью материала и наличие поверхностных дефектов могут привести к появлению дополнительных мест для адсорбции Н2. Учет возможности формирования второго слоя водорода дает значение сорбции Н2 на углеродной поверхности, равное ~ 4.1 % (мас.) [2].
Допирование графита щелочными металлами (K, Rb и Cs) несколько повышает его сорбционную способность. Для объяснения этого эффекта была выдвинута гипотеза, согласно которой щелочной металл катализирует частичное восстановление углерода в графитовом слое [87]. Тем не менее, к полученным в этой работе высоким значениям адсорбции Н2 относятся скептически [88, 109].
Для объяснения процесса поглощения водорода пучками углеродных НТ предложена модель, согласно которой водород рассматривается как сжимаемая жидкость, способная полностью заполнить свободное пространство внутри НТ. Использование значений плотности 0.071 г/см3 для жидкого водорода и 2.26 г/см3 для графита приводит к величине адсорбции Н2 внутри НТ, равной 2.3 % (мас.). Согласно другой модели, учитывающей адсорбцию молекул водорода с газокинетическим диаметром 0.289 нм как во внутренней полости НТ, так и в межтрубном пространстве жгутов из НТ (рис. 4.8), общая адсорбция Н2 для пучка из (10,10) НТ (D=1.38 нм) составляет
4.0 % (мас.), из которых 3.3 и 0.7 % (мас.) соответственно приходится на адсорбцию внутри трубок и между трубками в пучке. В условиях высокого давления сжимаемость водорода и учет межмолекулярного взаимодействия могли бы привести к более тесной упаковке молекул Н2 и, соответственно, к повышению его адсорбции на углеродных НТ. Для подтверждения этого предположения в [110] проведен детальный расчет, показывающий, что плотность водорода в этом случае может быть действительно выше, чем следует из чисто геометрических соображений.
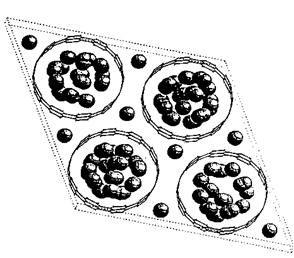
Рис. 4.8. Модель адсорбции молекул водорода в пучке ОНТ.
Выполнено также компьютерное моделирование адсорбции водорода на однослойных НТ и углеродном материале с идеализированными щелевидными порами [86]. Взаимодействия водород-водород и водород-углерод моделировались соответственно потенциалами Сильвера-Гольдмана и Кроула-Брауна; учитывались и квантовые эффекты. В расчетах предполагалась адсорбция водорода внутри НТ, между трубками и на внешней поверхности НТ. Компьютерное моделирование поглощения водорода углеродными НТ и активированным углем свидетельствует о преимуществе НТ, но не подтверждает высоких значений адсорбции водорода для ОНТ и ГНВ, найденных экспериментально [71, 81].
Расчеты адсорбции Н2 в пучках ОНТ показывают [86], что плотная упаковка приводит, тем не менее, к относительно низким значениям гравиметрической и объемной плотности водорода, даже при достаточно высоком адсорбционном потенциале. Низкое значение адсорбции может быть результатом недоступности внешней
поверхности в плотных пучках ОНТ. Результаты расчетов по методу Монте-Карло, проведенные для пучков, параллельно расположенных ОНТ, демонстрируют наличие сильной зависимости адсорбции водорода от диаметра пучка [111]. При 77 К и =10 МПа для изолированной (10,10) НТ и пучков, состоящих из трех и семи
(10,10) НТ, величина адсорбции Н2 составляет 9.6, 7.0 и 5.5 % (мас.) соответственно. Отмечено влияние на гравиметрическую емкость НТ расстояния между трубками в пучке.
Увеличение расстояния внутри пучков ОНТ, наблюдаемое при их обработке азотной кислотой [75], позволяет предположить, что параметр g = a – D, где g – ван-дер-ваальсова щель; a – постоянная решетки НТ; D – диаметр НТ, фигурирующий в расчетах адсорбции Н2, может быть оптимизирован [112]. Для достижения максимальной адсорбции водорода на ОНТ при 298 и 77 К проведена оптимизация геометрии упаковки (параметра g) для ОНТ. С этой целью изучен ряд НТ: (9,9) с D=1.22 нм, (12,12) с D=1.63 нм и (18,18) с D =2.44 нм, и найдено, что оптимальное значение g является функцией температуры и составляет соответственно 0.6 и 0.9 нм при 298 и 77 К.
Однако ни одна из изученных геометрий упаковки ОНТ (триангулярная и квадратная) не может привести при комнатной температуре к высоким значениям адсорбции водорода. Только при
77 К и > 5 МПа на углеродных НТ с D = 1.22 нм и g = 0.9 нм можно получить значения водородсорбционной емкости, приближающиеся к рекомендациям Международного энергетического агентства. Расчеты по методу Монте-Карло для заряженных углеродных НТ подтвердили некоторое увеличение их способности к поглощению Н2 по сравнению с незаряженными НТ: на 10-20 и 15-30 % для 298 и 77 К соответ¬ственно [113]. Однако весовая и объемная плотность водорода даже в случае заряженных НТ при 298 К все еще остаются слишком малыми.
Расчеты по методу сильной связи с использованием самосогласованного функционала плотности, выполненные с целью поиска оптимальных условий сорбции водорода углеродными ОНТ, показали, что на внешней и внутренней поверхностях НТ имеются два типа мест для хемосорбции Н2 [114]. На внешней поверхности ОНТ водород сорбируется в атомарном состоянии, а внутри канала ОНТ - в молекулярной форме [116] 1.
Появление в КР-спектре образцов НТ после их электрохимической зарядки новой полосы поглощения при 4226 см-1, отнесенной к поглощению молекулярного водорода (для газообразного Н2 – 4161 см-1), рассматривают как доказательство присутствия адсорбированного водорода. Емкость цилиндрических каналов углеродных ОНТ по Н2 растет линейно с диаметром трубки в соответствии с формулой Н2 (% (мас.)) 14.3 (D/Do), где 14.3 – % (мас.) поглощенного Н2 в (10,10) НТ, а Do – диаметр (10,10) НТ. Учет энергии межмолекулярного отталкивания молекул водорода во внутренней полости ОНТ, как и энергии взаимодействия молекула Н2 – стенка ОНТ, накладывает ограничение на величину максимальной сорбции Н2 углеродными НТ. Атомы водорода адсорбируются предпочтительно на внешней поверхности многослойных НТ, и сорбционная емкость МНТ по Н2 не зависит от их диаметра [116]. Максимальные расчетные емкости (5,5)@(10,10) МНТ и (10,10) ОНТ составляют соответственно 7.7 и 14.3 % (мас.) Н2 [114, 116].

